2023년 8월 15일, 국가약전위원회 공식사이트는 & ldquo;"중국약전" 9개 금속류 약포재 통칙 의견 청취에 관한 서한 & rdquo;2025년판'중국약전'에서 새로 수입한 5400의'약품포장용 금속부품과 용기'에 대한 의견을 수렴할 예정이며, 공시기간은 발표일로부터 1개월이다.이는 중국약전 2025판 약포재표준체계의 전반 계획과 편성구상에 근거한것이다.이 통칙은 약품포장시스템용 금속부품과 용기의 연구개발, 생산, 사용, 품질통제시 부합해야 할 기본요구를 규정하였으며 중방자문은 5400의"약품포장용 금속부품과 용기"요점을 정리하여 여러분들이 참고하도록 제공하였다.

1. 약품포장재료 이해 & mdash;—금속 포장 관련 용어
1. 약품 포장재
약칭약포재란 약품의 포장재와 용기에 직접 접촉하는것을 가리키는데 이는 약품을 환경의 영향으로부터 보호하고 약품의 원래의 속성을 유지할수 있다.약봉재는 약물제제의 중요한 구성부분으로서 합격된 약봉재는 약물제제가 그 치료효과를 발휘하도록 보장하는 전제이다.재료 구성에 따라 분류하면, 흔히 볼 수 있는 약봉지는 주로 6가지 종류의 품종 포장이 있다: 플라스틱 포장, 유리 포장, 고무 포장, 금속 포장, 사전 관개 포장 및 기타 포장.
2. 약품포장용 금속재료
정상적인 사용 조건에서 약품 포장에 사용되거나 이미 응용될 것으로 예상되는 각종 금속 (각종 금속 도금층 및 합금 및 함께 사용되는 금속 포함) 재료.
3. 약품 포장용 금속 부품
정상적인 사용 조건에서 약품 포장에 사용되거나 이미 응용될 것으로 예상되는 각종 금속 (각종 금속 도금층 및 합금 포함) 재료가 단조, 인장, 압연 등 공정 등을 거쳐 제조된 일정한 형식의 금속 포장 부품.
4. 약품포장용 금속용기
정상적인 사용조건에서 약품포장에 사용되였거나 이미 응용된 각종 금속 (각종 금속도금층 및 합금 포함) 재료로 만든 용기.
2. 약품포장용 금속부품과 용기의 품질통제요구에는 어떤 것들이 있는가?
금속 부품과 용기는 품질 위험 통제 등 요구에 따라 적당한 품질 요구 항목을 선택하고 제품의 기업 표준 또는 품질 협의를 제정하며 생산과 사용의 위험 관리 요구에 따라 검사 규칙을 제정해야 한다.생산 및 사용 과정에서 본 통칙의 규정을 포함하되 이에 국한되지 않는 특정 제제의 수요에 따라 품목 통칙 항목에서 적합한 항목을 선택하여 검사하여야 한다.안전과 직간접적으로 관련된 검사 항목에 대해 일반적으로 한도 지표를 사용하여 통제해야 하며 품질 제어 항목은 다음과 같다.
1. 감별
사용된 금속기재와 도금층 등 재료성분은 제품이 정의하거나 표시한 성분, 브랜드의 상응한 성분과 일치해야 하며 공급과 수요 쌍방이 확인한 검사빈도에 따라 금속기재는 금속재료원소함량측정법 (통칙 4250) 에 따라 성분과/또는 불순물함량은 기업표준 또는 품질협의 관련 규정에 부합되어야 한다.원료성분의 제한요구를 통해 원료생산공급업체의 공급사슬에서의 책임과 의무를 명확히 하며 원자재품질통제와 정보전달의 책임과 의무를 포함한다.
2. 이화학적 성능
금속류 재료의 핵심 품질 속성에 대해 제형의 위험 정도에 따라 제품 특징을 결합하여 관련 한도 지표를 구축한다.금속용기류 포장: 완전한 샘플의 적당량을 취하여 약포재 용출물 측정법 (통칙 4204) 에 따라 침출매체수, 4% 에틸산, 50% 에탄올을 표시용량 70 ℃ & plusmn에 관개한다.2 ℃ 는 24h 를 유지하고 침출매체 메탄으로 표시용량 58 ℃ & plusmn까지 주입한다.2 ℃ 는 24h 를 유지하고 약품 포장용 금속 부품과 용기 용출물 제조는 표 1을 참조한다.
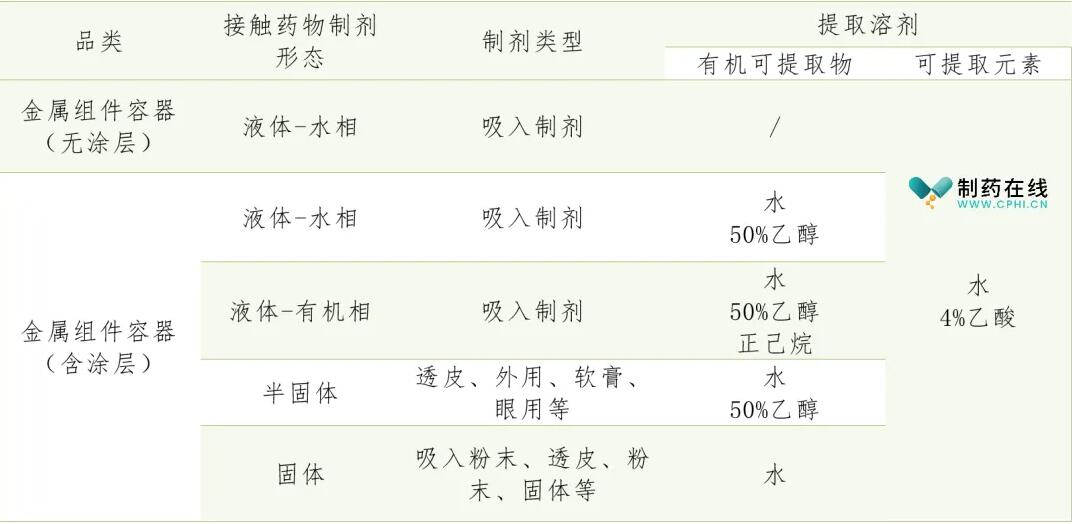
약봉지 용출물 측정법(통칙 4204)에 따라 다음 항목을 측정한다.
2.1 산화물
표1제비시료용액, 취수추출액약포장재용출물측정법(통칙4204)에 따라 측정하며 표2의 규정에 부합하여야 한다.
2.2 휘발물 없음 & nbsp;
표1에 따라 샘플 용액을 제조하고, 유기추출물 용액을 채취하여 약포재 용출물 측정법(통칙 4204)에 따라 표2의 규정에 부합하여야 한다.
2.3 총 유기탄소(TOC)
표1에 따라 샘플 용액을 제조하고, 취수 추출물 용액은 약포재 용출물 측정법(통칙 4204)에 따라 제약용수 중 총유기탄소 측정법(통칙 0682)을 참고한다.
2.4 금속이온 & nbsp;
현재 국내에서 이미 ICH Q3D 요구를 전환 응용하여 약품 중 유해원소에 대한 품질통제를 진행하고 있는 현황통칙 5400에 근거하여 금속이온검사항목을 추가하고 금속재료 조제방법 및 유해원소의 종류에 주목하며 1류, 2A류, 3류, 기타 원소에 따라 각각 관심 및 고찰원소의 범위 등을 구축한다.금속재료 조제 및 공정 중의 유해 원소 종류에 주목하고, 원소 불순물 검사는 ICH Q3D 원소 불순물 지도 원칙을 참조하여 흡입, 장외, 피부, 경피와 경구 약물 등 경로에서 원소 불순물을 추출하는 안전성 평가에 지도를 제공하며, 이미 알고 있거나 잠재적 인 원소 불순물의 출처를 식별하고, 약품 품질 요구와 결합하여 불순물 원소에 대해 위험 평가를 진행한다.ICH Q3D 원소 불순물 지침은 의약품 포장에 사용되는 금속 구성 요소 및 용기의 조제 구성이 알려져 있기 때문에 독성학이 주목하는 각 원소에 허용되는 일일 노출 (PDE) 을 설정하고 의약품의 원소 불순물을 통제하기 위해 위험 기반 방법을 사용합니다.
검수 기준: 표 1이 약품에 직접 접촉하는 약품 포장용 금속 부품과 용기 용출물 제조 시뮬레이션에 따라 적합한 침포 매체를 선택하고, 표 3을 참조하여 원소 평가를 진행하며, 추출 가능한 원소가 ICH Q3D 프로그램을 참조하여 일치하는 정량 독리학 안전 위험 평가를 진행하며, 상황을 참작하여 ICH Q3D PDE 값을 사용하고, 임계값 30%를 참조하여 특정 추출 가능한 원소를 제어할 필요가 있는지 여부를 확정하는 수단을 사용한다.동시에 표 3을 참조하여 재료 중의 기타 유형의 원소를 약품 제제 형식과 결합하여 평가 방법을 구축하고 포장 재료의 영향을 평가한다.
2.5 도료 단일 마이그레이션량
유기 코팅 도료를 사용하는 금속 부품과 포장에 대해 코팅 도료 단일체의 이동(비스페놀A, 파라벤, 아크릴산, 헥사메틸아미드, 부틸렌글리콜, 포름알데히드 등 *을 포함하되 이에 국한되지 않음)에 주목하고 표1에 따라 약품에 직접 접촉하는 약품 포장용 금속 부품과 용기 용출물 제조, 제형의 위험도에 근거하여 한도지표를 설정하고 품목통칙, 기업표준 또는 품질협의에 부합해야 한다.
참고*는 상기 코팅 도료 단체에 국한되지 않고 약봉재 생산과 사용자가 사용해야 할 코팅 도료 유형을 결합하여 적합한 코팅 도료 단체 표준과 지표를 제정하고 관련 협의를 제정한다.
2.6 내부 코팅 연속성
내코팅과 도금층을 사용하는 금속용기의 경우 금속내코팅 연속성 측정법(통칙 4058) 검사에 따라 측정전류는 40mA를 초과할 수 없습니다.
2.7 내부식 성능
적용 시 약품에 직접 접촉하는 금속 부품과 용기에 대해서는 금속 내부식 성능 측정법(통칙 4050) 검사에 따라 뚜렷한 부식이 없어야 한다.
3. 기타 요구 사항 & mdash;—무균, 미생물 한도 또는 생물학적 부하
실제 상황과 결합하여 서로 다른 용도 및 생산 사용 방식에 따라 상응하는 무균, 미생물 한도 또는 생물 부하 등을 선택하여 검사한다.